CCINP Physique et Chimie PSI 2019
| Thème de l'épreuve | Physique chimie et automobile |
| Principaux outils utilisés | mécanique des fluides, mécanique du point, électrocinétique, diagramme E-pH, solutions aqueuses, oxydoréduction |
| Mots clefs | portance, frottements, modulation d'amplitude, modulation de fréquence, plasma et ionosphère, accumulateur au plomb, alcoolémie, titrage, méthode de Cordebard |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - -
Énoncé complet
(télécharger le PDF)










Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
SESSION 2019 PSIPC03
GP
CONCOURS
COMMUN
INP
ÉPREUVE SPÉCIFIQUE - FILIÈRE PSI
PHYSIQUE - CHIMIE
Mardi 30 avril:8h-12h
N.B. : le candidat attachera la plus grande importance à la clarté, à la
précision et à la concision de
la rédaction. Si un candidat est amené à repérer ce qui peut lui sembler être
une erreur dénoncé, il le
signalera sur Sa copie et devra poursuivre sa composition en expliquant les
raisons des initiatives
qu'il a été amené à prendre.
Les calculatrices sont interdites
Le sujet est composé de quatre parties, toutes indépendantes.
Des données se trouvent en fin de sujet, page 12.
1/12
PHYSIQUE CHIMIE ET AUTOMOBILE
Partie I - Aspects aérodynamiques
La figure 1 montre l'allure des lignes de courant obtenues en soufflerie pour
deux
véhicules, l'un du type berline (semi-fastback) et l'autre correspondant à la
version à hayon
généralement dénommée break ou SW (hatchback). Les sections de référence et les
coefficients
aérodynamiques de ces deux véhicules sont un peu différents. L'écoulement de
l'air est supposé
incompressible.
Carrosserie semi-fastback
u Per:
RLELA A D
Figure 1 -- Essais en soufflerie
_ CxPoSV *
F, --
On rappelle l'expression de la force de traînée : , OÙ Po = 1,2 kg.m" est la
masse volumique de l'air, Vla vitesse relative de l'air par rapport à
l'obstacle, Cx le coefficient
aérodynamique de traînée de l'obstacle et S'la section de référence de
l'obstacle à l'écoulement.
Q1. Préciser les zones d'écoulement laminaire et turbulent. Quels sont les
facteurs qui influencent
le coefficient aérodynamique Cx.
On considère une automobile de masse mm = 1 300 kg, de coefficient
aérodynamique Cx= 0,33,
de section de référence S= 2,5 m° et dont le moteur développe une puissance P=
62,5 kW.
Q2. En négligeant dans cette question les frottements entre les pneumatiques et
la route et en
supposant l'air environnant au repos dans le référentiel terrestre, exprimer la
vitesse
maximale de l'automobile en fonction de tout ou partie des données précitées,
puis en donner
une valeur numérique en km/h.
Q3. Sur route ou autoroute, à vitesse stabilisée, la consommation en carburant,
exprimée en litres
pour 100 km parcourus, augmente en V*. Déterminer l'exposant x.
Pour améliorer la tenue de route, certaines voitures sportives sont équipées
d'un aileron pour
renforcer l'appui arrière (figure 2, page 3). On se propose 1c1 de quantifier
son influence.
2/12
Aileron
Figure 2 -- Aïleron arrière
L'air est assimilé à un fluide parfait. Son écoulement, dans le référentiel de
la voiture, est
supposé stationnaire et incompressible. L'effet de la pesanteur sur l'air est
négligé.
L'aileron, incliné vers le haut d'un angle non orienté f EUR or] par rapport à
la route,
dévie l'air qui s'écoule tangentiellement à la partie arrière du véhicule qui
est inclinée vers le bas
d'un angle, non orienté « EUR | par rapport à la route.
On note Se la section transverse de l'écoulement de l'air dévié par l'aileron.
Cette section est
supposée constante le long du tube de courant décrit sur la figure 3.
Flux d'air entrant
Aileron
Figure 3 -- Écoulement de l'air dans un tube de courant
On note respectivement V4 = ViUs et Ur = VoU, les vitesses des écoulements d'air
entrant et sortant du tube de courant. U, et U> sont des vecteurs unitaires.
On considère le système fermé, constitué par l'air compris entre les sections
AB et CD à la
date t et de l'air compris entre les sections A'B° et C'D" à la date t + dt.
Q4. On note dm1 la masse qui traverse la section AB entre t et t + dt et dmz la
masse qui traverse
la section CD entre t et t + dt. Comparer dm et dmz ainsi que V4 et U>.
3/12
Q5. En effectuant un bilan de quantité de mouvement sur le système fermé défini
précédemment,
déterminer la force exercée sur le tube de courant en fonction de Pp, V4, Se,
Vi et Vo.
Q6. On admet que la force F
r 9 _* 1°
irwénun EURXxercée par l'air sur le véhicule en mouvement est
l'opposée de celle exercée sur le tube de courant. En déduire la composante
perpendiculaire à
la route de la force exercée par l'air sur le véhicule en fonction de Do, V1,
Se, «à et f.
Discuter du sens de cette composante.
Partie II - Alimentation électrique
Compte-tenu de leur forte densité énergétique (150 W-h'kg'!), les batteries
lithium-ion sont
de plus en plus utilisées dans les véhicules électriques. Néanmoins, ces
batteries sont encore chères
et exposées à un fort risque d'explosion si elles sont rechargées dans de
mauvaises conditions.
Mise au point par le Français Gaston Planté en 1859, la batterie au plomb est
encore
aujourd'hui très compétitive et reste la principale technologie utilisée dans
les véhicules thermiques.
En effet, elle est capable de fournir un courant crête de grande intensité,
nécessaire pour le
démarrage électrique des moteurs à combustion interne.
Composition de l'atome de plomb
Q7. Préciser la composition du noyau de l'atome de plomb : "$2Pb.
Diagramme potentiel-pH du plomb
Le diagramme potentiel-pH, aussi dénommé diagramme £E-pH, simplifié du plomb,
tracé
pour une concentration égale à 10* mol-L'!, pour toute espèce soluble contenant
du plomb, est
représenté page 12. Les espèces prises en compte sont : Pb"*(aq), PbO(s),
PbO(s), HPbO2 (aq),
Pb(s) et Pb304(s).
Q8. Déterminer les nombres d'oxydation de l'élément plomb dans chacune des
espèces
considérées, puis reproduire sur votre copie ce diagramme £-pH du plomb, en
associant une
espèce à chacun des domaines d'existence ou de prédominance.
Le nombre d'oxydation du plomb dans l'espèce Pb;304(s) est-1l compatible avec la
quantification de la charge ? Proposer une explication.
Q9. Écrire les demi-équations redox dans lesquelles interviennent les deux
couples de l'eau. En
supposant toutes les pressions partielles égales à la pression standard P° = 1
bar, préciser les
équations des droites associées au diagramme Æ-pH de l'eau.
Q10. Superposer le diagramme £-pH de l'eau au diagramme ÆE-pH du plomb. Le
plomb est-1l stable
en solution aqueuse acide ? En solution aqueuse basique ? S1 non, écrire l'(es)
équation(s) de
la (des) réactions(s) chimique(s) qui se produi(sen)t.
Solubilité du sulfate de plomb dans une solution d'acide sulfurique
Q11. Déterminer, en faisant l'(es) approximation(s) qui s'impose(nt), la
solubilité s du sulfate de
plomb dans une solution d'acide sulfurique à 0,5 mol-L'!. Conclure.
4/12
Accumulateur au plomb en fonctionnement générateur
Les couples redox qui interviennent dans l'accumulateur au plomb (figure 4) sont
PbO:(s)/PbSO4(s) et PbSOA(s)/Pb(s).
E l 2,0 Charge électrique O
VO nr | |
PbSO4 |e SOA | so,
SO47 F
H>SOj/HO
Figure 4 -- Accumulateur au plomb
Q12. Écrire les deux demi-réactions chimiques, en fonctionnement générateur, en
précisant celle
qui a lieu à l'anode et celle qui a lieu à la cathode. En déduire la réaction
globale de
fonctionnement de l'accumulateur.
Q13. La tension ou force électromotrice d'un accumulateur au plomb dépend-elle
du pH? Si oui,
est-1l préférable d'utiliser dans l'accumulateur au plomb de l'acide sulfurique
très concentré
ou non ?
Masse d'une batterie au plomb
On désire réaliser une batterie au plomb dont la tension à vide Us est
supérieure à 12 V et
dont la capacité O est supérieure à 50 A.h.
On donne sur la figure 5, les courbes intensité-potentiel d'un élément de la
batterie utilisé
en mode décharge.
I (A)
À
Pb --+
1,68
> ÆE(V)
- 0,33
PbSO4 PbO>
Figure 5 -- Courbes intensité-potentiel
5/12
Q14. Quelle(s) grandeurs(s) électrique(s) de la batterie est (sont) modifiée(s)
par la mise en série de
£
plusieurs éléments ? Quelle(s) grandeurs(s) électrique(s) de la batterie est
(sont) modifiée(s)
par la mise en parallèle de plusieurs éléments ?
Q15. Combien faut-il associer d'éléments, en série, pour satisfaire le cahier
des charges ?
Q16. Exprimer la masse totale en plomb pur, solide, contenue dans la batterie
en fonction de la
capacité © de la batterie, de la constante F de Faraday et de la masse molaire
M{(Pb) du plomb.
Partie III - Aspects liés à la sécurité routière
III.1 - Limitations de vitesse
Dans cette sous-partie, 1l vous est demandé de faire preuve d'autonomie. Toute
démarche
même partielle de résolution sera prise en compte, pourvu qu'elle soit
cohérente.
Q17. Les causes d'accidents sont nombreuses et variées. Afin d'incriminer ou
non un éventuel
excès de vitesse lors de la sortie de route liée à un dépassement incontrôlé et
décrite sur la
photographie (figure 6), on vous demande de déterminer l'expression littérale,
puis
numérique de la vitesse du véhicule en début de la phase de freinage. Toutes
données
pertinentes et nécessaires à la résolution de cette question pourront être
introduites par le
candidat.
Figure 6 -- Sortie de route
6/12
Les éléments légaux de marquage au sol sont représentés sur la figure 7.
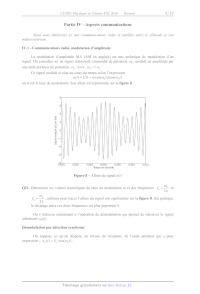
<----------> <-- 5 m 1,33 m + ne 3 m 3,5 m Figure 7 -- Législation de marquage au sol On rappelle qu'en cas de glissement, la réaction du sol sur les pneumatiques est décrite par la loi de Coulomb, à savoir: R=N+T, avec IT | = f LV |. T et N sont respectivement les composantes tangentielle et normale de la force À exercée par le support, f est le coefficient de frottement solide entre les pneumatiques et le revêtement de la chaussée. Par temps sec, on a : f-- 0,8. IIL.2 - Contrôle d'alcoolémie Principe L'éthanol contenu dans le sang peut être dosé par la méthode de Cordebard. L'éthanol (CH3CH20H) contenu dans le sang est séparé par distillation. Il est ensuite dosé à froid par une solution nitrochromique. Cette solution est un mélange d'acide nitrique (H°, NO3°) et de dichromate de potassium (2K*, CrÈ207") en excès. L'excès d'oxydant est ensuite dosé par iodométrie. Mode opératoire Q18. Un volume 5 de sang est dissout dans un volume , de solvant approprié (acide picrique). Après distillation, on récupère un volume V2 de distillat qui contient la totalité de l'alcool initial. Dans une fiole jaugée de volume V3, on introduit un volume /, de distillat et on complète jusqu'au trait de jauge avec la solution nitrochromique. On bouche la fiole jaugée et on laisse la réaction se dérouler pendant 5 minutes. On verse le contenu de la fiole dans un erlenmeyer, puis on ajoute de l'iodure de potassium en excès. On dose le diiode formé par une solution de thiosulfate de sodium (2Na*, S20:7) de concentration C6. On note V6 le volume équivalent. On recommence exactement le même protocole en remplaçant le distillat par de l'eau distillée. On note V:,7 le volume équivalent. Ecrire les réactions : de l'éthanol sur le dichromate de potassium ; de l'iodure de potassium sur le dichromate de potassium ; du diode sur le thiosulfate de sodium. Q19. Quelle est la couleur du diode en solution aqueuse ? Comment peut-on déceler l'équivalence du dosage du diode par le thiosulfate ? Q20. Déterminer la concentration Co, exprimée en mol:L'}, d'alcool dans le prélèvement de sang initial en fonction des différents volumes et de la concentration C4. 7/12 Partie IV - Aspects communications Nous nous limiterons ici aux communications radio et satellite entre le véhicule et son milieu exterieur. IV.1 - Communications radio, modulation d'amplitude La modulation d'amplitude MA (AM en anglais) est une technique de modulation d'un signal. On considère ic1 un signal informatif, sinusoïdal de pulsation &,, modulé en amplitude par une onde porteuse de pulsation &@,,avec ©, <<@,. Ce signal modulé évolue au cours du temps selon l'expression u(t)=U(I+mcos(@;f)) cos(o,f) où m est le taux de modulation. Son allure est représentée sur la figure 8. Signal modulé u(t) en Volt ©QO d || 0000 0.002 0.004 0.006 0.008 0.010 0.012 Temps en seconde Figure 8 -- Allure du signal w(f) Q21. Déterminer les valeurs numériques du taux de modulation m et des fréquences 7, = 5 et Î, = 37° utilisées pour tracer l'allure du signal z(t) représentée sur la figure 8. (En pratique, le décalage entre ces deux fréquences est plus important !) On s'intéresse maintenant à l'opération de démodulation qui permet de retrouver le signal informatif s/{t). Démodulation par détection synchrone On suppose ici qu'on dispose, au niveau du récepteur, de l'onde porteuse qui a pour expression : e,(f)=E, cos(®,f). 8/12 On envoie l'onde porteuse et le signal modulé dans un multiplieur, comme indiqué sur la figure 9. u(l) Sm() Multiplieur ep(t) Figure 9 --- Multiplication de l'onde porteuse et signal modulé Le multiplieur fournit en sortie la tension : sM(f) = K'u(f)'e,(f), où Æ est une constante dimensionnée. Q22. Préciser l'unité de Æ et donner simplement la valeur numérique de la constante Æ pour le multiplieur que vous avez dû utiliser en Travaux Pratiques. Q23. Déterminer l'expression du signal s,(t) délivré en sortie du multiplieur et représenter son spectre. On supposera 0 < m < 1 pour le tracé du spectre. Q24. Indiquer quelle(s) opération(s) de traitement du signal est (sont) encore nécessaire(s) pour retrouver le signal informatif s;/{#). IV.2 - Communications radio, modulation de fréquence On peut réaliser une modulation de fréquence MF (FM en anglais) suivant le schéma d'Armstrong (figure 10) qui utilise un montage intégrateur, un réseau déphaseur, un multiplieur et un soustracteur. Vine( [ ) V1(0)_ |" intégrateur (RC) Multiplieur V(t) OL V,( Soustracteur men V2(t) Déphaseur Va(t) Figure 10 -- Modulateur d'Armstrong Dans toute la suite, les Amplificateurs Linéaires Intégrés (ALT) sont supposés idéaux de gain infini et fonctionnent en régime linéaire. Le multiplhieur fournit en sortie la tension : V() = K:V{r)" Var). Le déphaseur est réglé pour provoquer un retard de phase de TA de la tension V4(t) par rapport à la tension V2({). On suppose qu'à f = 0, Vi(0) = 0. On impose par ailleurs, à l'entrée de l'ensemble, les deux tensions : V(/)=V, cos(@f) et V,(f)=V,, cos(o,f) avec: ©, >> @.
9/12
Étude du soustracteur
On considère le montage de la figure 11.
R2
R3
V,
Vn Va
R4
RER
Figure 11 -- Montage du soustracteur
Q25. Quelle considération de câblage permet de considérer ce montage comme
potentiellement
stable ?
Q26. Déterminer l'expression liant les différentes résistances R;, R2, R3, R,
et les tensions V,(t),
Va(t) et V;(t). Donner une condition simple entre R7, R2, R3 et Ripour que V
(f)=V,(#)---V,(#).
On considèrera par la suite cette relation vérifiée.
Étude de l'intégrateur
L'intégrateur est réalisé à partir d'un ALI, d'un condensateur de capacité C et
d'une
résistance À.
Q27. Proposer un schéma du montage intégrateur et préciser la relation
théorique qui lie V(t),
Étude du montage global
Q28. Montrer que la tension à la sortie du modulateur d'Armstrong peut se
mettre sous la forme :
(9 =, J1+8° sin? (of) sin(@,f + p().
Préciser les expressions de & et de tan(o(f))en fonction de #, Vi», R, C, @, et
de f.
Q29. Lorsque £& et o(f) sont petits devant 1, la tension de sortie peut se
mettre sous la forme
V (4) =V,, sn(o,f+msin(@t)) = V,, sin(y(t))
où @,est la pulsation élevée de la porteuse, m le taux de modulation de
pulsation modulante
@, et wy(f) la phase instantanée.
Préciser l'expression de m en fonction de k, Vi», R, Cet ©.
10/12
Q30. On appelle pulsation instantanée du signal P,({) la grandeur : A(f) = vo .
Établir la
relation liant Q(f), ©,,k, R, Cet Vr(t). Justifier le nom de modulation de
fréquence associé à
ce traitement du signal.
IV.3 - Effet de l'ionosphère, positionnement satellite et taille des antennes
L'ionosphère est la couche atmosphérique comprise entre 60 km et 800 km
d'altitude.
Exposée au rayonnement solaire, elle s'ionise et constitue un plasma. Pour les
ondes
électromagnétiques, l'ionosphère est un milieu dispersif. La relation de
dispersion est de la forme
2 2
k° ... @ -- © rasma
= 2
C
où oeest la pulsation de l'onde électromagnétique, ©
lasma la pulsation propre du plasma et c la
célérité de la lumière dans le vide.
On a © = 27 f susma AVEC
plasma
de l'ordre de 10 MHz.
plasma
Q31. Parmi les deux fréquences suivantes f1 -- 162 kHz et f; = 1 227 MHZ,
déterminer celle qui
correspond à une fréquence radio MA et celle utilisée pour les communications
par satellite.
Q32. L'une des antennes les plus utilisées dans les équipements portables est
l'antenne "quart d'onde",
sa longueur théorique est d'un quart de longueur d'onde. Déterminer l'ordre de
grandeur de la
longueur d'une antenne de voiture, susceptible de capter les ondes MF (FM en
anglais), dont
la fréquence de la porteuse est de l'ordre de 100 MHZ. Avez-vous déjà prêté
attention à
l'antenne du dispositif du système GPS ? Qu'en déduisez-vous ?
11/12
Diagramme E-pH du plomb
E(V) î
1,5
1,25
0,75
0,5
0,25
- 0,25
Données
Formules trigonométriques
V(a,b) EUR R°,ona:
acos0+ bsinO = Va + b? sin(0+ op)
a
b
\/a° +b° Va" + b°
cos a°cos b = 72 (cos(a - b) + cos(a + b))
avec COS p = et sin@ =
Données thermodynamiques à 298 K
L'acide sulfurique H2S0O4 est un diacide dont
les deux acidités sont considérées comme
fortes, 1l s'ionise donc deux fois totalement
en solution aqueuse.
Produit de solubilité :
K(PbSO4(s)) = 1,6 10*.
Potentiels redox :
EH"(aq)/H2(g)) = 0,00 V.
E°(CH3COOH(aq)/CH3CEHOH(aq)) = 0,03 V.
E°(S106/(aq)/S2037(aq)) = 0,09 V.
E°(L(aq)/T(aq)) = 0,62 V.
E°(O02(g)/H0) = 1,23 V.
E(CnO7"(aq)/Cr'*(aq)) = 1,33 V.
(RTIn10Y/F = 0,06 V/unité de pH.
FIN
12/12
IMPRIMERIE NATIONALE - 191156 - D'après documents fournis