Centrale Physique et Chimie 1 PSI 2023
| Thème de l'épreuve | Utilisation des batteries Li-ion |
| Principaux outils utilisés | diffusion thermique, thermodynamique, mécanique des fluides, électronique de puissance, cinétique chimique, oxydoréduction, courbes courant-potentiel |
| Mots clefs | hacheur, transfert conducto-convectif, loi de Fourier, batterie, lithium, Li-ion, accumulateur, explosion, emballement thermique |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)






Rapport du jury
(télécharger le PDF)





Énoncé obtenu par reconnaissance optique des caractères
Physique-chimie 1
PSI
4 heures Calculatrice autorisée
2023
Utilisation des batteries Li-ion
Ce sujet aborde quelques éléments liés à l'utilisation des batteries
lithium-ion. À partir d'une première étude
chimique et thermodynamique sur un accumulateur en fonctionnement, on
s'intéresse à la diffusion thermique
dans une batterie composée d'un ensemble d'accumulateurs. Enfin, une dernière
partie aborde l'utilisation de
panneaux solaires comme source d'énergie. Les trois parties sont largement
indépendantes.
Certaines questions, peu ou pas guidées, demandent de l'initiative de la part
du candidat. Leur énoncé est repéré
par une barre en marge. Il est alors demandé d'expliciter clairement la
démarche, les choix et de les illustrer,
le cas échéant, par un schéma. Le barème valorise la prise d'initiative et
tient compte du temps nécessaire à la
résolution de ces questions.
Un formulaire et certaines valeurs numériques sont regroupés en fin d'énoncé.
I Étude d'un accumulateur Li-ion
Figure 1 Accumulateur Li-ion de type 18650
IA --- Accumulateur lithium fer phosphate
Les batteries Li-ion LiFePO,/C ont une densité d'énergie quatre fois supérieure
à celle des batteries au plomb.
Elles sont actuellement utilisées dans les voitures électriques et les
smartphones. Un accumulateur est constitué
d'une électrode en lithium fer phosphate (LiFePO;) et d'une électrode de
graphite (C). En fonctionnement,
l'électrode LiFePO, ne peut pas être complètement dé-lithiée et la quantité de
matière en ions Lit effectivement
extraite est de seulement 0,6 mol. On considère que les deux demi-équations
suivantes modélisent les réactions
qui se déroulent aux électrodes :
LiFePO,{, -- 0,6 Lit + 0,6 e + Lis aFePO;( (L.1)
Lit +6 Ces + EUR -- LiCs(s) (12)
Q 1. Identifier, en justifiant, la réaction se déroulant à l'anode et celle à
la cathode.
Q 2. Écrire l'équation bilan de la pile en fonctionnement.
Q 3. En utilisant une approche électrochimique, proposer une estimation de la
masse d'un accumulateur
18650 de capacité spécifique 2600 mAh.
Q 4. La masse d'un tel accumulateur est mesurée à m = 45,5 g. Proposer une
explication de la différence
avec la masse obtenue à la question précédente.
I.B - Courbe galvanostatique
Des courbes densité de courant-potentiel, comme celle simplifiée proposée en
figure 2, permettent de mieux
connaitre les limites de l'électrode employée. Le solvant utilisé est
l'éthyl-propyl-carbonate (EPC) dont le do-
maine d'inertie électrochimique est compris entre les potentiels Egpc1 = -3,0 V
et Egpc2 = 2,1 V. Par
convention, l'abscisse des courbes densité de courant-potentiel utilisant le
lithium est le potentiel évalué par
rapport au potentiel standard du couple Li*/Li,,,.
Q 5. Décrire le montage à trois électrodes permettant de tracer une courbe
courant-potentiel.
Q 6. Attribuer à la portion (a) de la courbe la demi-équation d'oxydoréduction
susceptible de se produire
en s'appuyant notamment sur les données numériques.
La diminution de courant sur la portion (b) est attribuée à un phénomène de
passivation à la surface de
l'électrode accompagné d'une transition de phase.
Q 7. Proposer une explication de l'augmentation brutale de la densité de
courant sur la portion (c) de la
courbe.
P054/2023-03-15 18:56:08 Page 1/9 CIEL
450 |
400 |
3D0 |
300
')
250 |
200 |
150
; fa /
j (mA-cm ?)
JÙ
0
2,9 3,0 3,90 4,0 4,5 9,0 9,9 6,0
E -- Eu (V)
Figure 2 Courbe densité de courant-potentiel simplifiée d'une électrode de
LiFePO,;,,, le
solvant utilisé est l'éthyl-propyl-carbonate (EPC) contenant des ions Li à 1
mol-L'
Q 8. Tracer l'allure de la branche de réduction du couple Lif /LiC (s) pour une
électrode en graphite
plongeant dans de l''EPC avec une concentration en ions Lit de C, = 4,0 mol-L
!. On supposera que le couple
considéré correspond à un système rapide. Justifier l'intérêt d'utiliser des
concentrations élevées.
IC - Échauffement d'un accumulateur
I.C.1) Thermodynamique physique
Depuis l'utilisation de ces batteries Li-ion, plusieurs cas d'explosion ont été
recensés que ce soit pour les té-
léphones portables, les ordinateurs ou encore les véhicules. Des
courts-circuits au sein de l'accumulateur ont
souvent été incriminés. En 2011, des chercheurs Taïwanais ont montré que
lorsque la température dépasse 100 °C,
les accumulateurs Li-ion peuvent exploser et induire localement une élévation
de température de 900 °C.
Q 9. Estimer le temps de décharge d'une batterie Li-ion mise en court-circuit
dont la résistance interne est
r = 7,7 m(, la tension à vide U = 3,7 V et la capacité spécifique 2600 mA:h.
Q 10. Déterminer s'il est possible qu'un court-circuit puisse être responsable
d'une telle élévation de tempé-
rature.
I.C.2) Influence de l'électrolyte
Ces chercheurs ont constaté que l'explosion d'une batterie Li-ion peut survenir
même pour un accumulateur
déchargé. Parmi les réactions intervenant dans les explosions de batteries
Li-ion, la combustion de l'acide
pyruvique (C;:H,03 a): utilisé comme électrolyte, joue un rôle important dans
l'élévation de température. Sa
réaction de combustion est modélisée par l'équation
D
9 O; (g) + CsH03 (1) ---- J CO; (g) + 2 HO, (L.3)
Q 11. Justifer que l'enthalpie standard de formation de O,,,, est nulle.
Q 12. Déterminer l'enthalpie standard de réaction à 298 K. Commenter son signe.
Afin d'évaluer les risques lors d'une surchauffe d'une batterie Li-ion, un
accumulateur de type 18650 initialement
à la température 7; -- 298 K sous une pression P: = 1,0 bar est placé dans un
calorimètre en acier fermé
hermétiquement de volume V, = 150 mL (figure 3). Le système est équipé d'une
mesure en temps réel de la
température et de la pression malgré l'explosion. Cette batterie est chauffée
progressivement jusqu'à 4, = 129°C,
température à partir de laquelle l'explosion de la batterie commence. Dans
toute l'étude, on suppose que la
capacité thermique du calorimètre est négligeable et que le volume occupé par
la batterie est négligeable devant
l'espace libre disponible. En outre, on considère les gaz comme parfaits.
P054/2023-03-15 18:56:08 Page 2/9 (cc) BY-NC-SA
vanne de
sécurité D
| thermocouple
P CET e
transducteur
de pression
Vo
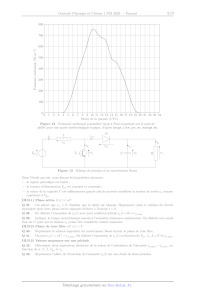
Figure 3 Vent Sizing Package 2 (VSP2), calorimètre adiabatique
à faible inertie thermique, d'après https://www.fauske.com
Q 13. Déterminer, compte tenu de l'évolution de la température observée (figure
4), si le calorimètre est
parfaitement calorifugé.
Q 14. En estimant le temps caractéristique de retour à la température ambiante,
justifier que la transforma-
tion du contenu du calorimètre liée à l'explosion peut être assimilée à une
transformation adiabatique.
1000
900
SUU
700
600 |
© 900 |
100 |
300 \
; \
100 TT -- NC
TT a
Û s1Ù 100 150 200 290 300 JOÛ AOÛ
t (min)
0
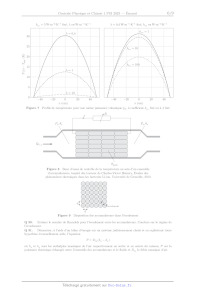
Figure 4 Profil de température d'une batterie chauffée dans un calorimètre,
d'après Can-Yong Jhu et al, Journal of Hazardous Materials, 2011
On suppose notamment que
-- ]a contribution des gaz enfermés dans l'enceinte est négligeable en termes
de bilan thermique :
-- l'énergie libérée lors de l'explosion correspond en bonne approximation à
l'échange thermique isotherme à
pression constante associé à la réaction (1.3) :
-- le dioxygène nécessaire à la réaction (1.3) est fourni en quantité juste
suffisante par une décomposition interne
de l'accumulateur.
Q 15. En utilisant la figure 4, estimer la quantité de matière d'acide
pyruvique mise en jeu lors de l'explosion.
Q 16. Déterminer la quantité de matière d'acide pyruvique nG,nH,0, 1im
conduisant à la pression pi, = 75bar
dans le calorimètre.
Q 17. Sachant que le calorimètre utilisé peut résister à une pression de 75
bar, conclure quant à l'intérêt
d'un des éléments constitutifs du calorimètre schématisé sur la figure 3.
P054/2023-03-15 18:56:08 Page 3/9 (cc) BY-NC-SA
I.D --- Emballement thermique
On suppose que la réaction de combustion de l'électrolyte (L.3) suit une loi de
vitesse d'ordre 1 par rapport à
l'acide pyruvique C:H,0:. On considère que les réactifs sont introduits en
proportions stoechiométriques dans
un volume V constant. On note a4:.(t) le taux d'avancement de la réaction comme
rapport de la quantité de
matière en acide pyruvique consommé par la quantité de matière initiale, notée
n,.
Q 18. Exprimer la loi de vitesse donnant la vitesse de disparition de l'acide
pyruvique en fonction de aq, (t);
no. V et la constante de vitesse k.
Q 19. Rappeler la loi d'Arrhénius. Préciser l'influence de la température sur
la vitesse de réaction.
Q 20. On considère une batterie de capacité thermique ©, siège de la réaction
(1.3) de combustion de l'électro-
lyte. On décompose la transformation adiabatique entre t et t+dt en une
transformation chimique à température
et pression constantes puis un échauffement isobare de la batterie. Exprimer la
variation d'enthalpie lors de ces
deux transformations infinitésimales. Montrer que l'évolution de température
vérifie :
ar E
ne -- 1] -- . --_ 4
dt 5 Qiss) EXP | ex)
où 5 est une constante positive à exprimer en fonction des constantes et
données du problème.
Q 21. Au regard de l'équation différentielle ci-dessus, justifier le terme
d'emballement thermique lorsque
l'avancement de la réaction est faible (aq. & 1).
Le dispositif expérimental décrit figure 3 permet de relever la température en
fonction du temps notamment
pour aqu(t) & 1. La figure 5 donne une représentation de In _ en fonction de L.
7.0
6,5
6,0
5,5
5.0
7 4,5
Ë 4,0
© 9,0
z 3,0
5e 2
-- 2,0
SR 15
£ 1,0
0,5
0,0
--0,5
1.90 1.95 2.00 2.05 2.10 2 15
1000/T (K-!)
Figure 5 Tracé de In(d7'/dt) en fonction de 1000/T° pour une batterie Li-ion
déchargée
pendant son explosion, d'après Can-Yong Jhu et al, Journal of Hazardous
Materials, 2011
Q 22. En supposant que le modèle isobare reste valide, calculer l'énergie
d'activation à l'aide de la courbe
de la figure 5.
II Contrôle thermique d'un ensemble d'éléments
Une batterie d'une voiture électrique est composée d'environ 2000 éléments et
représente une part non négligeable
du prix du véhicule. Le contrôle de la température a pour but d'optimiser les
performances de la batterie, tout
en limitant son vieillissement. Un système de gestion thermique de batterie
idéal permet :
-- d'éviter à la batterie de subir des températures extrêmes (inférieures à
--30 °C et au-delà de 40 °C) :
-- de minimiser l'écart de température entre les accumulateurs à 10 °C ;
-- de conserver une température moyenne dans le pack aux alentours de 25 à 30
°C.
Le premier point permet d'éviter la dégradation de la batterie et de ses
performances. L'uniformisation de la
température des cellules accorde tous les accumulateurs au même niveau de
performance pendant toute la durée
de vie de la batterie. Enfin, la gamme de température moyenne proposée permet
d'associer des performances
optimales vis-à-vis du fonctionnement de la batterie et de sa durée de vie.
P054/2023-03-15 18:56:08 Page 4/9 (cc) BY-NC-SA
IT. À -- Diffusion thermique
On considère un ensemble d'accumulateurs Li-ion en série formant un bloc
cylindrique homogène de rayon a et
de longueur 2L = 1,00 m. Le tout est plongé dans l'air considéré comme un
thermostat à la température T\,,.
On suppose le gradient radial de température suffisamment faible pour que, dans
la section droite d'abscisse x,
la température T'(x,t) soit uniforme. On note y la masse volumique de
l'accumulateur cylindrique, EUR sa capacité
thermique massique et À sa conductivité thermique ; ces trois grandeurs sont
constantes et uniformes.
En fonctionnement en régime permanent, chaque accumulateur dégage une puissance
par unité de volume » 7,
uniforme et constante, notamment en raison de l'effet Joule. On note À. le
coefficient conducto-convectif à
travers la surface latérale de sorte que la loi de Newton pour l'interface
accumulateur-fluide s'écrive
J = PAUAEZ t) EH Text )ü
où ü est le vecteur unitaire local, normal à la surface latérale, orienté vers
le fluide.
moteur
Lx
' T'(x,t) 24
Rec / |
CZ x
î
| > T
-- L 0 L
Figure 6 Notations
Q 23. À partir d'un bilan d'énergie sur un système judicieusement choisi,
montrer que le champ de tempé-
rature vérifie l'équation aux dérivées partielles suivante :
OT'(x,t) OT(x,t) 2h
-- © = À ---- LT --T(x,t)) +pr.
[1228 dt O1? + a ( ext (x )) PJ
Q 24. Simplifier l'équation précédente en régime stationnaire, en faisant
apparaitre les grandeurs A -- ee
CC
et T; -- Laxt + D.
CC
Q 25. Préciser la signification physique de la grandeur H.
Q 26. On admet que T'(x = +L) = T,,. En déduire que le profil de température
peut se mettre sous la
forme
T(x) = Acosh (5) +B
où À et B seront des constantes exprimées en fonction de À}, L, Te... et T1.
Q 27. Ce modèle a permis de construire les représentations graphiques
présentées figure 7. Commenter
qualitativement ces simulations au regard des expressions de À et 7}. Parmi les
valeurs proposées pour les
paramètres À et h.. de ces simulations, préciser lesquelles permettraient de
contribuer à une bonne gestion
thermique de la batterie.
IIB - Étude sur banc d'essai
Afin d'assurer le bon fonctionnement d'une batterie, la température des
différents éléments peut être contrôlée
grâce à un flux d'air circulant autour des éléments. Afin d'évaluer les
échanges thermiques avec l'air, un ensemble
de N = 144 accumulateurs de type 18650 (de diamètre d = 18 mm) sont superposés
les uns aux autres et
placés dans un caisson ventilé et calorifugé, de section parfaitement adaptée à
la dimension du pack (figure 8).
L'écoulement de l'air, supposé stationnaire et incompressible, est assuré par
un ventilateur imposant un débit
volumique en entrée de Q,,, = 80 m°-h *. Des instruments de mesure permettent
d'évaluer la température de
l'air à l'entrée du caisson (9, = 20,0 °C) ainsi qu'à sa sortie (0, = 25,5 °C).
Q 28. Les différents accumulateurs sont placés côté à côte selon un agencement
6 x 6 x 4 (figures 8 et 9).
Exprimer puis calculer d la distance caractéristique de l'écoulement entre les
éléments.
EUR
écoulement :
Q 29. Estimer la vitesse de l'écoulement entre les accumulateurs, en supposant
l'écoulement parfait.
P054/2023-03-15 18:56:08 Page 5/9 (cc) BY-NC-SA
T(x) En L'ext (K)
Q 30.
30
29
20
15
10
h.. = 5 W:m *K | fixé, À en W:m !-K-1{ À =0,4W:m !K | fixé, h,. en W:m ?K7{
h..=1
= 04 ce
Djocosseee portes LS \
--40 -- 20 Û 20 40
x (cm)
Qv,e --+
Re nn
D --------
------------
it --
LAURE
\
Ô
Le
©
Q
À
Figure 8 Banc d'essai de contrôle de la température au sein d'un ensemble
d'accumulateurs, inspiré des travaux de Charles-Victor Hémery, Études des
phénomènes thermiques dans les batteries Li-ion, Université de Grenoble, 2013
écoulement
Figure 9 Disposition des accumulateurs dans l'écoulement
Estimer le nombre de Reynolds pour l'écoulement entre les accumulateurs.
Conclure sur le régime de
l'écoulement.
Q 31.
Démontrer, à l'aide d'un bilan d'énergie sur un système judicieusement choisi
et en explicitant toute
hypothèse éventuellement utile, l'équation
P -- D, (h, -- h.)
où À, et À, sont les enthalpies massiques de l'air respectivement en sortie et
en entrée du caisson, P est la
puissance thermique échangée entre l'ensemble des accumulateurs et le fluide et
D,,
P054/2023-03-15 18:56:08
le débit massique d'air.
Page 6/9 CITES
Q 32. Déterminer l'expression de la puissance échangée entre l'ensemble des
accumulateurs et l'air supposé
se comporter comme un gaz parfait, puis calculer sa valeur numérique à partir
des mesures de températures 0,
et 0...
Q 33. En fonctionnement, la température du pack est mesurée à 0, -- 30,0 °C et
est supposée uniforme
sur l'ensemble du pack. On note 0 = (0, + 0.,)/2, la température moyenne de
l'air circulant autour du pack.
Estimer la valeur du coefficient conducto-convectif h..
Q 34. Les manomètres mesurent une chute de pression AP = 10 mbar de part et
d'autre des accumulateurs.
Expliquer l'origine de cette variation de pression.
Q 35. Exprimer puis calculer la puissance électrique consommée par le
ventilateur en considérant que le
rendement électromécanique du ventilateur vaut 60%. Commenter ce résultat.
III Utilisation de panneaux solaires
III. À -- Puissance nécessaire pour une voiture
Q 36. On considère le véhicule présenté figure 10 roulant sur un sol
horizontal. En admettant que les frot-
tements de l'air sont prépondérants devant toute autre forme de dissipation
d'énergie et à l'aide des figures 11
et 12, proposer une estimation de la vitesse maximale que peut atteindre ce
véhicule, sans tenir compte de la
présence de tout dispositif de stockage d'énergie.
Figure 10 La société néerlandaise Lightyear propose une berline équipée
de 5 m° de panneaux solaires qui mesure 5,05 m de longueur, 1,82 m de
largeur et 1,40 m de hauteur et possède un coefficient de trainée C, = 0,23
Les cellules solaires en tandem qui associent le silicium à une pérovskite aux
halogénures
métalliques constituent une voie prometteuse pour dépasser la limite
d'efficacité des cellules
individuelles. Nous décrivons un tandem pérovskite/silicium monolithique avec
un rendement
de conversion de puissance certifié de 29,15%. L'absorbeur de pérovskite, avec
une bande
interdite de 1,68 eV, est resté stable en phase sous illumination grâce à une
combinaison
d'extraction rapide des trous et de recombinaison non radiative minimisée à
l'interface sélective
des trous. Ces caractéristiques ont été rendues possibles par une monocouche de
carbazole
à substitution méthyle auto-assemblée comme couche sélective de trous dans la
cellule de
pérovskite. L'extraction accélérée des trous était liée à un faible facteur
d'idéalité de 1,26 et
à des facteurs de remplissage à jonction unique allant jusqu'à 84%, tout en
permettant une
tension en circuit ouvert en tandem pouvant atteindre 1,92 V. À l'air, sans
encapsulation, un
tandem conserve 95 % de son efficacité initiale après 300 heures de
fonctionnement.
Figure 11 Résumé de l'article de Amran AlAshouri et al., publié dans Science en
décembre 2020
ITI.B --- Conversion de puissance
La tension V,, fournie par les panneaux solaires ne permet pas de recharger
directement une batterie de ten-
sion 350 V. Un régulateur MPPT (Maximum Power Point Tracking) constitué d'un
convertisseur électronique
DC/DC a pour rôle d'optimiser les valeurs des paramètres électriques de
fonctionnement entre le système photo-
voltaïque et la batterie. Le champ d'application de ces convertisseurs est
large ; on étudie ici un hacheur parallèle
(convertisseur Boost) dont le schéma de principe est donné en figure 18.
Ce système est composé principalement d'une bobine d'inductance L et de deux
interrupteurs 7, et D considérés
comme idéaux. Le conducteur ohmique de résistance À modélise la batterie à
charger. Un signal rectangulaire
périodique de période T commande l'interrupteur 7. Selon l'état des deux
interrupteurs, on peut distinguer
deux phases de fonctionnement :
-- la phase active, de durée aT', lorsque l'interrupteur T°. est fermé et
l'interrupteur D est ouvert : le coefficient
a désigne le rapport cyclique ;
-- la phase de roue libre, de durée (1 -- a)T', lorsque l'interrupteur T,. est
ouvert et l'interrupteur D est fermé.
Page 7/9 CIEL
P054/2023-03-15 18:56:08
SUU
700 / S
600 \
500 / CC
400 \
/ \
300 / \
0 \
100 / \
0 Ne
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24
Heure de la journée (UTC)
Figure 12 Puissance surfacique journalière reçue à Paris moyennée sur le mois de
juillet pour une année météorologique typique, d'après
https://re.jrc.ec.europa.eu
Puissance surfacique (W:m ?)
D
in NL 1D | |
-- LT i,
tr Un Yo
210 r jte. ete all
Figure 13 Schéma de principe d'un convertisseur Boost
Dans l'étude qui suit, nous faisons les hypothèses suivantes :
-- le régime périodique est établi :
-- la tension d'alimentation V,., est continue et constante ;
-- la valeur de la capacité C est suffisamment grande afin de pouvoir
considérer la tension de sortie v, comme
supérieure à V,..
III.B.1) Phase active 0 0. Justifier que la diode est bloquée. Représenter
alors le schéma du circuit
équivalent pour cette phase active supposée débuter à l'instant t = (0.
Q 38. En déduire l'expression de 7, (t) avec pour condition initiale 47 (t = 0)
= iz in:
Q 39. Indiquer le temps caractéristique associé à l'ensemble
résistance-condensateur. En déduire une condi-
tion sur C pour que la tension v, puisse être considérée comme constante.
III.B.2) Phase de roue libre aT