Centrale Physique et Chimie 1 PSI 2024
| Thème de l'épreuve | Autour d'une centrale nucléaire |
| Principaux outils utilisés | thermodynamique, induction électromagnétique, bilans en système ouvert, solutions aqueuses, python |
| Mots clefs | diffusion thermique, cycle thermodynamique, diagramme des frigoristes, premier principe industriel, précipitation, précipité, solubilité, oxyde de nickel |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)









Rapport du jury
(télécharger le PDF)







Énoncé obtenu par reconnaissance optique des caractères
Physique-Chimie 1 à
Ps! ©
4 heures Calculatrice autorisée ON
Autour d'une centrale nucléaire
Une centrale nucléaire utilise l'énergie dégagée par la fission nucléaire des
atomes d'uranium placés au coeur
du réacteur. La chaleur générée par la fission est transférée à un fluide
caloporteur, généralement de l'eau qui
circule dans le circuit primaire. L'eau du circuit primaire est portée à très
haute température par l'effet des
réactions de fission nucléaire qui ont lieu au sein du coeur du réacteur. Elle
passe ensuite dans un pressuriseur
qui maintient sa pression constante et égale à p = 155 bar, puis effectue un
échange thermique avec le circuit
secondaire dans un générateur de vapeur : l'énergie thermique dégagée par l'eau
du premier circuit vaporise
alors l'eau du second, qui fait ensuite tourner plusieurs turbines génératrices
d'énergie mécanique, elle-même
enfin transformée en énergie électrique par un alternateur.
BÂTIMENT RÉACTEUR
(ZONE NUCLÉAIRE
Circuit secondaire
>
A
J SALLE DES MACHINES
(ZONE NON NUCLÉAIRE)
Crayons
combustiles .
Turbine
fl | x | Alternateur
-- f
D
Cie d | ee Condenseur
uve au D)
D 4 réacteur ÿ L
Y . . ° Je
ne s Circuit.de refroidissement
Circuit primaire D
* --,
Pompe ®) ® =
FLEUVE OÙ MER
Figure 1 Principe d'un réacteur nucléaire. Librement adapté d'une illustration
EDF.
Certaines questions, repérées par une barre en marge, ne sont pas guidées et
demandent de l'initiative de la
part du candidat. Les pistes de recherche doivent être consignées par le
candidat sur sa copie ; si elles sont
pertinentes, elles seront valorisées. Le barème tient compte du temps
nécessaire pour explorer ces pistes et
élaborer un raisonnement, il valorise ces questions de façon très significative.
Un formulaire et certaines données numériques sont disponibles en fin d'énoncé.
I Étude du circuit primaire
Le coeur est constitué de N -- 41448 crayons combustibles. Chaque crayon
combustible est constitué d'un
cylindre de hauteur H = 3,66 m et de diamètre d = 2R, = 9,5 mm. Ces crayons
sont le siège de réactions de
fission, exothermiques.
La puissance thermique développée dans le coeur vaut : P, = 2776 MW.
P053/2024-05-03 11:42:51 Page 1/12 (@} sY-Nc-saA
Le circuit primaire doit être correctement dimensionné pour prévenir tout
échauffement anormal du com-
bustible, UO; 4. dont la température de fusion vaut 2800 °C. La conductivité
thermique de UO: vaut
À = 3,5 W-m !K 1.
La pression de vapeur saturante de l'eau à 345 °C vaut 155 bar.
Dans cette partie, on se place en régime stationnaire et on néglige les
variations d'énergie mécanique.
I.A -- Évolution de la température entre le coeur du combustible et le fluide
caloporteur
On étudie l'évolution de la température entre le centre du combustible UO: et
l'eau du circuit primaire,
qui circule dans l'espace annulaire de rayon allant de À, à À; et entourant les
crayons. On suppose que la
température du fluide caloporteur est une constante et vaut 7: = 303 °C.
On note 7, et T, les températures de part et d'autre de l'interface entre le
combustible et la gaine. On note 7},
et 7; les températures de part et d'autre de l'interface entre la gaine et le
fluide caloporteur.
Pour simplifier, on néglige les effets de bord à chaque extrémité des cylindres
; on considère pour l'étude que les
N crayons combustibles de hauteur H sont disposés les uns au-dessus des autres
et que les échanges thermiques
se font exclusivement selon une direction radiale.
Les échanges thermiques au niveau d'une interface sont modélisés selon la
relation de Newton : la puissance
thermique traversant une surface dS de cette interface s'écrit hdS (T°, -- T°)
où À désigne le coefficient de
transfert conducto-convectif et 7°, et 7}, désignent les températures de part
et d'autre de l'interface.
Le coefficient de transfert conducto-convectif entre le combustible et la gaine
vaut h, = 10 kW:m *-K {. Le
coefficient de transfert conducto-convectif entre la gaine et le fluide
caloporteur vaut h; = 25 kW:m *.K {.
Chaque crayon est entouré d'une gaine d'épaisseur e = À, -- R; = 0,60 mm dont
la conductivité thermique vaut
À3 = 16 W:m :K f.
| |
d |
« * gaine :
| | gaine
| |
| |
| 2
1; L:|13
| | TT:
I I
I I UO
I I
u . 2(5) "
: |: |é :
I I
H £ | à VO, , | & R È
© I Ù © 3 ©
e! , : 8, a.
© = =
S |, | Ô R, 5
(ob I I D) D)
E DE EE, -.! e =
= AT TT TT US = R =
H |,71,- INT E 5 OE
= X------- > T
Figure 2
Q 1. Exprimer la surface latérale totale, notée $S,,.,, de l'ensemble des N
crayons combustibles entourés de
la gaine en fonction de N, d et H.
On note P,, la puissance thermique par unité de volume engendrée par les
réactions de fission au coeur des
crayons combustibles et que l'on suppose uniforme. On appelle r la distance à
l'axe du cylindre modélisant
l'ensemble des N crayons.
Q 2. Montrer que l'équation de la diffusion thermique vérifiée par la
température dans le combustible
s'écrit :
d dT
-- | 7 -- Ar = (,.
dr ra) + Ar = Û
Exprimer À en fonction de P,, et À.
P053/2024-05-03 11:42:51 Page 2/12 (CO) BY-Nc-SA |
Q 3. Exprimer la température T(r) dans UO,,,, en fonction de P,, T:, R3, À et r.
Q 4. Exprimer la température 7, en fonction de 7;,, P,, h;, d, e, Het N.
Q 5. Exprimer la température T'(r) en un point de la gaine en fonction de 7,
P,, R,, À, Si et r.
Q 6. Calculer les températures 7°,, T,, T, et 7°.
Q 7. Représenter le profil température T(r) pour 0 < r < R+k. Q 8. Expliquer pourquoi le bon fonctionnement du pressuriseur du circuit primaire fait partie des critères majeurs de sureté. Proposer une solution pour pouvoir évacuer une puissance plus importante. I.B --- Prise en compte de dépendances longitudinales pour la puissance thermique volumique et la température Dans cette partie, on néglige l'influence de la gaine mais on tient compte du profil non uniforme, selon la coordonnée 2, de la puissance thermique générée par les réactions de fission, ainsi que de la dépendance avec z du champ de température. Chaque crayon combustible de rayon À, et de hauteur H est refroidi par une circulation d'eau liquide dans un espace annulaire de rayon extérieur À; entourant le crayon. On ne considère dans cette sous-partie qu'un seul crayon. Figure 3 La puissance thermique P,{2) par unité de volume engendrée par les réactions de fission au sein de la barre du FH combustible est modélisée par : P,{2) = P, sin ( HF ). On suppose que les échanges thermiques se font toujours exclusivement dans la direction radiale de la barre de combustible. On appelle r la distance à l'axe du cylindre. L'eau liquide cireule à la vitesse v = 5,0 m:s ! avec un débit massique D,, = 0,30 kgs ! ; la température d'entrée (en z = 0) de l'eau liquide est 7°, = 284 °C et sa température de sortie (en z = H) est T, = 322 °C. La capacité thermique massique de l'eau liquide, supposée constante sur cette plage de température, est prise égale à EUR; = 5750 J-K-l-kg!. On admet qu'il n'y a pas d'échange thermique avec l'extérieur pour r = Rÿ. Dans la suite, on suppose que la température de l'eau liquide ne dépend que de z et on la note T(z): la température dans la barre de combustible dépend de r et z et est notée T7, (r,2). Q 9. En réalisant un bilan thermodynamique pendant dt pour l'eau liquide entre les cotes z et z+ dz (avec dz & z), en écoulement stationnaire dans l'espace annulaire, justifier que : D, c; [T(z + dz) -- T(2)] = P,(2)rR,dz. Q 10. Exprimer 7°, -- T° en fonction de R,, H, D,,, c; et F,. Exprimer la température T'(2) de l'eau liquide en fonction de 7°, T°, z et H. On note h.. le coefficient de transfert conducto-convectif entre la barre de combustible et l'eau liquide dans ce modèle, et T,,(z) la température de la paroi de la barre de combustible à l'altitude 2. Q 11. Montrer que: TZ) --T 1 me = ;|[1+Bcos (%) + C'sin (u)] Exprimer B et C'en fonction de h., À, D,,, & et Ru. CC? P053/2024-05-03 11:42:51 Page 3/12 (CO) BY-Nc-SA | Q 12. Déterminer la température T'.(r,z) dans la barre de combustible. Montrer que : T(r,2)--T, 1 T2 r2 _ (TZ TT. = ;h+nee (5 )]+fe+r(-)]sn (Te). Exprimer D, E et F'en fonction de D, c;, H,h., À et Ri. Q 13. Exprimer la température T°,.(r = 0,2) sur l'axe de la barre de combustible à l'altitude z en fonction de 7°, T,, D,,, 2, H, GG, Re, Ào et Ri. M ? CC? Q 14. En déduire l'altitude pour laquelle la température sur l'axe de la barre de combustible est maximale. Calculer la valeur de la température maximale sur l'axe ; on prendra À, = 33 kW :m *-K !. Préciser si un critère de sureté en température est respecté. Le graphe de la figure 4 représente l'évolution de la température de la paroi du crayon combustible avec la cote Z. Q 15. Justifier qualitativement son allure. 340 330 __ 320 © % 310 LS 300 290 0 0,5 1 1,5 9 2,5 3 3,5 Cote z(m) Figure 4 Évolution spatiale de la température T,, de la paroï du crayon combustible. II Étude du circuit secondaire IT. À --- Préliminaire On considère un fluide en écoulement stationnaire, sans variation notable de son énergie mécanique, dans une machine. Il y entre dans l'état E (pression p,,, température 7°,, enthalpie massique h,) et en sort dans l'état $ (pression p,, température T°, enthalpie massique h,). On note w, le travail utile massique et q le transfert thermique massique reçus algébriquement par le fluide lors de la traversée de la machine. Q 16. Établir soigneusement la relation vérifiée dans ce cas par À, -- h,, w, et q. II.B -- Cycle de Hirn On considère le circuit secondaire, décrit par la figure 5 : -- la pompe d'alimentation porte l'eau liquide juste saturée (état 0) de la basse pression p3 -- 0,040 bar du condenseur à la pression p, -- 85,8 bar du générateur de vapeur (GV) de façon isentropique (état 1) : -- l'eau liquide entre ensuite dans le générateur de vapeur, où elle est chauffée de façon isobare jusqu'à la température 1, du changement d'état (état 1' -- liquide juste saturant), puis est totalement vaporisée jusqu'à l'état 2 (vapeur saturante sèche). Le surchauffeur (2 -- 2°') fonctionne de façon isobare : -- la vapeur sèche produite (état 2') subit ensuite une détente isentropique dans une turbine calorifugée amenant le système dans l'état 3, à la température T, : -- le mélange diphasé (état 3) pénètre ensuite dans le condenseur pour y être totalement condensé (état 0). P053/2024-05-03 11:42:51 Page 4/12 (CO) BY-Nc-SA | 2 9° | ( Alternat Surchauffeur erna = 3 | Condenseur 4 E Eau de circulation 1' il ( 7? | >
Générateur de vapeur
Pompe d'alimentation
Figure 5 Cycle de Hirn.
On se place en régime stationnaire. On suppose l'eau liquide incompressible et
on néglige le travail consommé
par la pompe devant les autres termes énergétiques de l'installation.
Dans la suite, les grandeurs thermodynamiques indicées par ? sont relatives à
l'état 2.
On donne 7, = 7, = 29°C, 7, = 300 °C et 7,, = 500 °C, ainsi qu'un extrait de
tables thermodynamiques pour
l'eau sur le tableau 1. Les données suivantes sont également fournies :
-- chaleur latente massique de vaporisation de l'eau à T, : L,(T,) = 1404
kJ-kg! ;
-- enthalpie et entropie massiques respectives de la vapeur d'eau sèche à 500
°C et 85,8 bar : À = 3391 kJ-kg |
et s -- 6,68 kJ-kg -K |.
Pression de vapeur Température Liquide juste saturé Vapeur saturante sèche
saturante (bar) (°C) s h s h
85,8 300 3,25 1345 5,70
0,040 29 0,42 121 8,47 2554
Tableau 1 Quelques données thermodynamiques pour l'eau. L'enthalpie
massique À est exprimée en kJ-kg"! et l'entropie massique en kJ-kg"!-K"f.
Q 17. Expliquer pourquoi 7, = T, et h, © h,. Préciser l'allure d'une
transformation isentropique dans le
domaine liquide du diagramme des frigoristes (p, h).
Q 18. Donner le nom des différentes courbes du diagramme des frigoristes (p, h)
du document réponse 1 et
y représenter précisément le cycle décrit par le fluide.
Q 19. Calculer, à partir de données du tableau 1 pour plus de précision, le
titre massique en vapeur ainsi
que l'enthalpie massique de la vapeur à la sortie de la turbine. Positionner le
point représentatif de cet état sur
le diagramme des frigoristes du document réponse 1.
Q 20.
Q 21. Établir l'expression de l'efficacité de Carnot ne d'une machine cyclique
ditherme fonctionnant en
moteur entre une source chaude à la température 7% et une source froide à la
température T}. La calculer en
prenant respectivement pour 7, et T4 les températures minimale et maximale du
fluide dans le circuit secondaire.
Commenter en justifiant l'écart éventuel avec la valeur de l'efficacité obtenue
à la question précédente.
Définir et calculer l'efficacité n de ce cycle.
ITI.C -- Cycle à double surchauffe
Les gouttes d'eau liquide peuvent endommager la turbine. Aussi, est-il
avantageux d'utiliser une turbine à deux
corps permettant d'obtenir un titre massique en vapeur en sortie de turbine
proche de 1 grâce à une double
surchauffe. Le cycle de Hirn précédent est modifié :
-- de l'eau (état 1) est admise dans le générateur de vapeur (GV) d'où elle
sort à l'état de vapeur saturante
sèche (état 2) :
-- elle passe ensuite dans le premier surchauffeur isobare (2 -- 2'), pour être
détendue dans la turbine haute
pression (HP) (2° -- 4):
-- la vapeur sèche (état 4) est envoyée dans un second surchauffeur isobare (4
-- 4') pour être ensuite détendue
dans l'étage de turbine basse pression (BP) (4 --5). Le titre massique en
vapeur dans l'état 5 est sensiblement
égal à 1 ;
Page 5/12 (@)sY-Nc-sAa
P053/2024-05-03 11:42:51
-- le fluide dans l'état 5 se condense totalement à la température 7, dans le
condenseur isobare (5 -- 0) :
-- Je liquide juste saturé (état 0) est ensuite comprimé de façon isentropique
à la pression p, du générateur de
vapeur (état 1).
Les détentes dans les turbines, calorifugées, sont supposées isentropiques. On
se place encore une fois en régime
stationnaire et on a toujours 7, = 15 = 29°C, 7, = 300°C et T;, = 500 °C. De
plus, 7, = 300°C et 74, = 500°C.
Q 22. Représenter précisément le cycle décrit par le fluide dans le diagramme
des frigoristes du document
réponse 1. Définir et calculer l'efficacité de de cycle.
II.D -- Cycle réel d'une tranche nucléaire
Pour des raisons technologiques, des limitations de pression et de température
interviennent directement dans
le choix des caractéristiques du cycle eau-vapeur de ces centrales thermiques
nucléaires, d'où des cycles moins
« poussés » que dans les centrales thermiques classiques.
Le coeur du réacteur est réfrigéré et modéré par l'eau, laquelle vient se
refroidir dans les échangeurs principaux
(appelés générateurs de vapeur). Les mélangeurs ou réchauffeurs sont notés R1,
R2, R3, R4, R5 et R6 (figure 6).
On se place toujours en régime stationnaire.
|
I I > Sécheur-Surchauffeur
Eau du_ : Y
circuit \
primairé URL LT ne Lo Alternateur
) HP BP
Echangeurs a ee ES ne _ 2-2 -
LT , =
' ù_ y
Condenseur
| R4A R3 R2 R1. ; a)
Pompe Pompe
Figure 6 Schéma simplifié du circuit eau-vapeur d'une centrale nucléaire.
Q 23. Calculer l'efficacité du cycle en vous appuyant notamment sur les
caractéristiques thermodynamiques
du cycle fournies dans le tableau 2. En déduire la puissance disponible aux
bornes de l'alternateur. En réalité,
cette puissance disponible n'est que de 960 MW : proposer une explication.
P053/2024-05-03 11:42:51 Page 6/12 (CO) BY-Nc-SA |
.... Débit massique Température Pression Enthalpie massique
Eau du circuit (th) (°C) (bar) KJ-ke 1)
Eau sortie condenseur 32,9 0,050 136,0
Eau sortie réchauffeur 4 181,1 768,0
Eau sortie réchauffeur 5 181,7 772,2
Pau entrée 5412,1 219.3 60 041,7
échangeurs principaux
_... Vapeur sortie 5412,1 268,7 54 27884
échangeurs principaux
Vapeur admission
turbine HP 5001,9 266,4 52 2787,1
Vapeur alimentant le 403.7 266.4 59 27871
sécheur surchauffeur
Vapeur soutirage 6
sortie turbine HP 214,3 223,3 26 2682,
Vapeur soutirage 5
sortie turbine IP 208,4 203,4 17,6 2622,6
Vapeur soutirage 4
sortie turbine IP 402,1 183,8 11,5 2562,8
Vapeur à l'échappement
de la turbine HP 4177,1 183,8 11,5 2562,8
Vapeur admission
turbine BP 3704,0 264,1 11,2 2970,4
Vapeur soutirage 281,4 137,8 3.6 2731.5
3 sortie turbine
Vapeur soutirage 235.4 97,4 0,97 2538,9
2 sortie turbine
Vapeur soutirage 134,2 60.8 0,22 2377.8
1 sortie turbine
Vapeur entrée condenseur
(en provenance 3033,0 32,9 0,050 2242 ,2
de la turbine BP)
Tableau 2 Caractéristiques thermodynamiques du cycle.
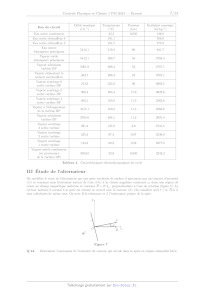
III Étude de l'alternateur
On modélise le rotor de l'alternateur par une spire circulaire de surface $
parcourue par un courant d'intensité
i(t) et tournant sans frottement autour de l'axe (Oz) à la vitesse angulaire
constante w, dans une région où
existe un champ magnétique uniforme et constant B=B ü.. perpendiculaire à l'axe
de rotation (figure 7). Le
vecteur unitaire n normal à la spire est orienté en accord avec le courant
i(t). On considère qu'à t = 0, Bet ñ
sont colinéaires de même sens. On note À la résistance et L l'inductance propre
de la spire.
U à
3
ut
eIRé
Figure 7
& Y
Q 24. Déterminer l'expression de l'intensité du courant qui circule dans la
spire en régime sinusoïdal forcé.
P053/2024-05-03 11:42:51
Page 7/12
CETTE
Q 25. Obtenir l'expression de la valeur moyenne de la projection sur l'axe (Oz)
du moment du couple exercé
par B sur la spire en rotation. Interpréter son signe.
Q 26. Déterminer la puissance mécanique moyenne de la turbine qui entraîne le
rotor de cet alternateur,
ainsi que la puissance moyenne dissipée par effet Joule. Comparer ces deux
puissances.
IV Contrôle de la concentration en bore dans le circuit primaire
Chaque réacteur nucléaire est équipé d'un circuit de refroidissement du
réacteur à l'arrêt. Ce circuit contient
un mélange d'eau et de bore. Le bore, présent dans l'eau du circuit primaire
sous forme d'acide borique dissous,
permet de modérer, par sa capacité à absorber les neutrons, la réaction en
chaîne. Les règles d'exploitation
demandent de réaliser un contrôle de la concentration en bore.
L'acide borique H,BO, est un monoacide faible :
H3BO 3 (ag) + 2H20 = B(OH), (39) + H3O ag) avec pK, = 9,25 à 25 °C.
IV.A --- Titrage pH-métrique
En présence de D-mannitol (noté M), l'ion B(OH),_ donne un ion noté C7. La
dissociation de H,BO, avec le
D-mannitol s'écrit :
H3BO 34) + 2H20 -- B(OH), (aa) + H3O7 (aa) (IV.1)
B(OH), (ao) +2Mao = C' tag) + 44H20 (IV.2)
La constante thermodynamique d'équilibre de la réaction IV.2 est K, -- 10°.
Q 27. Calculer la constante d'équilibre K de la réaction de formation de CO
(ag): avec un coefficient stoechio-
métrique unité, à partir de l'acide borique et du D-mannitol aqueux à 25 °C.
Commenter le résultat.
Le mélange H3BO3 {44 +2 Mag) joue le rôle d'un acide faible au sens de
Bronsted. On définit la constante d'acidité
_ 4c- dx,0+
a,app
apparente de l'acide borique par K où interviennent les activités des espèces
dissoutes.
dH,BO;
Q 28. Exprimer pK en fonction de pK = --logK, M, et de la concentration
standard c°.
a,apP aq)
On étudie le dosage de l'acide borique par une solution d'hydroxyde de sodium.
On prépare 10 mL d'une solution d'acide borique de concentration ©, : on ajoute
+ grammes de D-mannitol en
s'assurant de respecter la condition Mao) > [H3BO3 (ao) ; on complète à 200 mL
avec de l'eau distillée. On
ajoute un barreau aimanté afin d'agiter le mélange.
On dispose dans la burette d'une solution d'hydroxyde de sodium à la
concentration CZ = 0,10 mol-L !. On
appelle VA le volume de la solution d'hydroxyde de sodium versé au cours du
dosage.
On réalise trois dosages à 25°C avec des valeurs différentes de x, l'une
d'elles correspondant au cas x = 0 (absence
de D-mannitol). Les trois courbes (a), (b) et (c) correspondantes, obtenues
suite à une étude expérimentale,
figurent sur le graphe de la figure &.
Q 29. Déterminer C, ainsi que les valeurs de x notées respectivement x,, x, et
x, ayant conduit à chacune
des courbes (a), (b) et (c).
IV.B - Titrage conductimétrique
On s'intéresse à présent au principe d'une autre technique de titrage,
conductimétrique.
On prépare 10 mL d'une solution d'acide borique de concentration C7} ; on la
complète avec de l'eau distillée
jusqu'à atteindre un volume V, -- 40 mL où la concentration en acide borique
est notée C1. On ajoute un
barreau aïmanté.
Dans la burette, on dispose d'une solution titrante d'hydroxyde de sodium à la
concentration C3 = 0,10mol-L À.
On appelle V, le volume de cette solution titrante versé au cours du dosage à
25 °C.
On utilise un conductimètre pour suivre l'évolution de la conductivité o de la
solution titrée en fonction du
volume V3.
P053/2024-05-03 11:42:51 Page 8/12 (CO) BY-Nc-SA |
Q 30. Déterminer la loi de conductivité o en fonction notamment du volume VA de
solution titrante versé
avant et après l'équivalence.
Q 31. Représenter, justifications à l'appui, l'allure de (V, + VA) o en
fonction de VA en y repérant le volume
réel versé VA 4 à l'équivalence. Conclure sur la possibilité de titrer ainsi le
bore en solution.
12
" (a)
sers (b)
-- (CC
= À (c)
er
6},
4
2
Û 2 4 6 8 10 12 14 16 18 20
V3 (mL)
Figure 8 Courbe de titrage pH-métrique de l'acide borique,
avec ou sans D-mannitol, par l'hydroxyde de sodium.
V Étude de la contamination des circuits par les produits d'activa-
tion
Un flux de neutrons peut activer des atomes qui produisent alors un
rayonnement. Les tubes des générateurs de
vapeur sont constitués d'Inconel (alliage à base de nickel et de chrome). La
composition massique de l'alliage
690 est : 58 % de Ni, 31 % de Cr et 11 % de Fe. Les alliages à base de nickel
jouent un rôle important dans
la construction des matériaux utilisés pour le circuit primaire. De nombreuses
études (Palmer, Tremaine et
Leblanc, etc.) ont été menées sur la solubilité des oxydes métalliques (Ni, Fe,
Cr, Co). On étudie par la suite
l'oxyde de nickel NiO,,,.
V.A --- Préliminaire
Q 32. Représenter un diagramme de prédominance ou d'existence en fonction du
pH relatif aux espèces
NiO,; Ni (ag) à une température de 300°C. On prendra une concentration de
frontière C;. = 1,0x 10 "mol-L 7.
Q 33. Expliquer l'origine de l'irradiation possible des intervenants lors des
opérations de maintenance dans
le circuit primaire et la préconisation du choix d'un pH supérieur à 3 dans
l'eau du circuit primaire à une
température de 300 °C.
V.B - Modéle de Palmer
On considère les espèces NiO!,,; Ni
S -- INT ao + INI(OH sta a):
ag) EUR Ni(OH ag) On note s la solubilité de l'oxyde de nickel définie par
Q 34. Représenter un diagramme de prédominance en fonction du PH relatif cette
fois-ci aux espèces Ni"
et Ni(OH)o{aa) à la température de 300 °C.
aq)
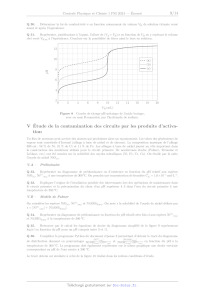
Q 35. Retrouver par le calcul les équations de droite du diagramme simplifié de
la figure 9 représentant
log(s) en fonction du pH pour un pH compris entre 3 et 11.
Q 36. Compléter le programme Python du document réponse 2 permettant d'obtenir
le tracé du diagramme
Le . [NI (ac [Ni(OH)s (ac) . N
de distribution donnant en pourcentages NOM au INT qui et NOM ana INA al Cl
fonction du pH à la
température de 300 °C. Le programme doit également représenter sur le même
graphique une droite verticale
correspondant au pH de l'eau neutre à 300 °C.
Le tracé obtenu est similaire à celui de la figure 10 réalisé dans les mêmes
conditions d'étude.
P053/2024-05-03 11:42:51 Page 9/12 (CO) BY-Nc-SA |
2 3 4 0 6 7 8 9 10 11 12
pH
Figure 9 Diagramme de solubilité de l'espèce NiO,,, en fonction du pH à 300 °C.
100 PR RO ER ER ES EE EE RS
80
60
7
40
20
2 3 4 D ( 7 8 9 10 11 12
pH
Figure 10 Diagramme de distribution à 300 °C.
V.C - Modéle de Tremaine et Leblanc
Les mesures de Tremaïne et Leblanc montrent que la dissolution de l'oxyde de
nickel atteint un palier minimum
à 300 °C entre les pH 7 et 8 avant d'augmenter à nouveau. L'espèce Ni(OH); 0)
est postulée pour justifier cette
augmentation de la solubilité au-delà de pH = 8.
+
On appelle K,, la constante thermodynamique d'équilibre de la réaction :
NiO,,,+3 H,0 -- Ni(OH)30) +H30
Pour T' = 300 °C, on a K,3 = 1,699 x 107 À.
Q 37. Représenter un diagramme de prédominance en fonction du pH relatif aux
espèces NET ao): Ni(OH) (ao)
et Ni(OH) 30 à la température de 300 °C.
La solubilité de l'oxyde de nickel est cette fois-ci définie par s = [Ni] +
[Ni(OH oo) + IN(OH)
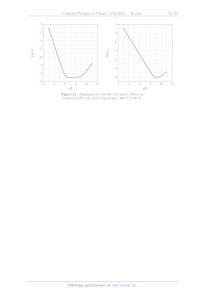
Le diagramme de solubilité de l'oxyde de nickel est représenté sur la figure 11
pour deux températures différentes.
Q 38. Déterminer par le calcul les valeurs de pH où la solubilité est minimale
pour les températures de 300°C
et 90 °C. On négligera les variations de K., avec la température.
Lors d'un arrêt à froid, la pression du circuit primaire peut descendre jusqu'à
31 bar et la température jusqu'à
90 °C.
Q 39. Expliquer pourquoi il est essentiel de bien choisir le pH lors du
fonctionnement en puissance du circuit
primaire. Préciser une valeur optimale du pH relativement au nickel. Citer
le(s) risque(s) encouru(s) par le
personnel lors des opérations de maintenance si le pH n'est pas modifié lors de
l'arrêt à froid.
P053/2024-05-03 11:42:51 Page 10/12 CEE
log (s)
12
10 12
pH
pH
Figure 11 Diagramme de solubilité de l'espèce NiO(s) en
fonction du pH pour deux températures : 300 °C et 90 °C.
Page 11/12
P053/2024-05-03 11:42:51
CETTE
Formulaire et données
Opérateur gradient en coordonnées cylindriques :
10f.
of _
r 06 0
-- ÿ..
Oz *
Of
---- U
d Ô
gra f(r, ,z) = Or
FT
Variation d'entropie d'une phase condensée incompressible de capacité thermique
Centre un état 1 et un état 2:
AS = Clin 22.
nn
Coordonnées du point critique de l'eau : T4 = 374°C, pc = 221 bar.
I
Formule trigonométrique : sin & Sin b -- 5 [-- cos(a + b) + cos(a -- b)|.
Moment du couple subi par un dipôle magnétique en champ magnétique uniforme : l
=M AB.
Loi de Kohlrausch : o -- >, À,C;, avec © la conductivité de la solution et À;
la conductivité molaire ionique de
l'ion d'indice ? de concentration C;.
Tableau de conductivités molaires ioniques à 25 °C :
Ion H3,07* Na* OH B(OH),
À;
(mS-m2mol 1) 39,0 5,01 19,8 6,70
Produit ionique de l'eau à plusieurs températures :
Température
o 25 90 300
(°C)
pK, 14,00 12,44 11,41
Équations de réaction et lois d'évolution de leur pK avec la température T'en
kelvins :
5513, 46
: + EL .2+ EL .
NiO,,, + 2H,0,,, -- Ni (aq) +- 3H,0 PK4 --= 6, 093 -- D.
Ni'? 4 H,0 = Ni(OH 2H,0* K-: -- --6,09 1282, 1 0,009476T
1 {aq) + 2 -- i( )a(aq) + 3 (aq) P£É5 -- 0; + T + U,
Autres données numériques :
Grandeur Notation Valeur Unité
Masse molaire de l'acide borique MyBo, 61,84 g-mol |
Masse molaire du D-mannitol M, 182,17 g-mol !
Constante des gaz parfaits R 8,314 J-K !mol |
Concentration standard C° 1 mol-L |
ee oerINeee
Page 12/12 @evncsa
P053/2024-05-03 11:42:51
R 718 Ref :W.C.Reynolds: Thermodynamic properties in SI
DTU, Department of Energy Engineering
S in [KJ/(kg K)]. T in [°C]
M.J. Skovrup & H.J.H Knudsen.
DOCUMENT RÉPONSE 1
200,000
100,006-
80,000-
60,000-
40,000-
20,000-
18
10,006-
8,000-
6,000-
4,000-
N
©O
©
©O
]
Pression [Bar]
1,80 2,40 3,00 3,60 4,20 4,80 5,40 6,00
1000
1600 14
En
Diagramme d
s = 0,60 1,20
1200 1400
200 400 600 800
La pression est exprimée en bar, l'entropie massique en kJ-kg"
.P*lJ1Lh _úSPLa1 R
R718 Ref :W.C.Reynolds: Thermodynamic properties in SI
200,000 DTU, Department of Energy Engineering
s in [kJ/(kg K)]. T in [ºC]
M.J. Skovrup & H.J.H Knudsen.
340
320
36
300
100,000
80,000
60,000
280
260
240
40,000
220
200
20,000
180
10,000
8,000
6,000
160
140
Pression [Bar]
4,000
120
2,000
100
1,000
0,800
0,600
80
0,400
60
0,200
0,100
0,080
0,060
40
0,040
20
0,020
0,010
s = 0,60 1,20
0
200
1,80
400
2,40
600
3,00
800
3,60
4,20
1000
1200
4,80
1400
5,40
6,00
1600
18
En
.B;`KK2 /
G T`2bbBQM 2bi 2tT`BKû2 2M #`- H2Mi`QTB2 KbbB[m2 2M L+LH
luatex 1.14 20210305 MKIV
Ne rien écrire dans la partie barrée
P053-DR/2024-04-08 10:29:23
DOCUMENT RÉPONSE 2
1
2
3
4
5)
imp
imp
# F
def
ort numpy as np
ort matplotlib.pyplot as plt
onctions de calcul des constantes d'équilibre K4 et K5 associées respectivement
à pK4 et pK5
KA(T): # Température T en kelvins
return
def K5(T): # Température T en kelvins
return
# Température en kelvins
T =
# Valeur du pH de l'eau neutre à la température T
pHen =
N = 1000 # Nombre de points
pHmin = 3 # pH de départ pour la représentation
pHmax = 11 # pH de fin pour la représentation
pas = (pHmax-pHmin)/(N-1) # Pas entre deux valeurs successives du pH
pH = np.zeros(N) # Tableau de N valeurs nulles
yi = np.zeros(N)
y2 = np.zeros(N)
for i in range(N):
pHlil = pHmin+ti*pas # Valeur du pH pour le point d'indice i
h = 10*x(-PH[i]l) # Valeur de h=[H30+]/c°
# Part yi = [Ni2+]/C[Ni(OH)2]+[Ni2+])
yili]l =
# Part y2 = [Ni(OH)2]/C[NiC(OH)2]+[Ni2+])
y2[il =
# Réalisation du tracé en fonction du pH
# avec une ordonnée en pourcentage (valeurs comprises entre O et 100)
pit
pit
pit
pit
pit
pit
pit
pit.
.figure()
.plot( ) # Courbe relative à [Ni2+]/([Ni(OH)2]+[Ni2+])
.plot( , linestyle='--') # Courbe relative à [Ni(OH)2]/([Ni(OH)2]+[Ni2+])
.plot([pHen, pHenl, [0, 100], linestyle=':') # Courbe relative au pH de l'eau
neutre
.xlabel('pH')
.ylabel('7')
.grid() # Affichage de la grille
show()