Centrale Physique et Chimie 2 PSI 2018
| Thème de l'épreuve | L'oxygène |
| Principaux outils utilisés | thermodynamique, mécanique des fluides, électromagnétisme, électronique, oxydoréduction, thermochimie |
| Mots clefs | brayton, climatisation, capteur, paramagnétisme, photodiode, oxygène, modèle atmosphérique, aviation, chlorate de sodium, analyseur de gaz, oxyde de zirconium |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- -
Énoncé complet
(télécharger le PDF)





Rapport du jury
(télécharger le PDF)



Énoncé obtenu par reconnaissance optique des caractères
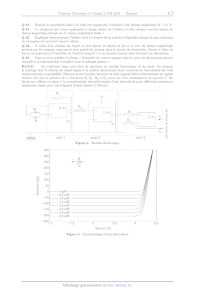
t'» Physique--Chimie 2 00 °.) , !--l _/ PSI @ cnucuuns EENTHHLE--SUPËLEE 4 heures Calculatrices autorisées N Ce sujet porte sur l'oxygène que l'on respire : les ressources et les moyens de les exploiter, ainsi que la mesure du taux de dioxygène. Les données numériques sont regroupées en fin d'énoneé. I L'oxygène: ressources, production I.A * L'oxygène est présent dans l'atmosphère (où la fraction molaire en dioxygène est très proche de 21%), dans les océans (il constitue 86,0% de la masse de l'eau de mer) et dans la croûte terrestre dont il est le principal élément (voir données en fin de sujet). Q 1. Que vaut le pourcentage massique en oxygène dans l'eau pure '? Q 2. En déduire la teneur globale, exprimée en gL", de l'ensemble des autres constituants de l'eau de mer. Q 3. Citer, en donnant leur formule chimique, deux oxydes présents dans la croûte terrestre qui y expliquent la présence d'oxygène. On se place dans un modèle d'atmosphère isotherme. On considère que la pression au niveau du sol vaut P0 : lbar et que la composition de l'atmosphère ne varie pas avec l'altitude : l'air est considéré comme un gaz parfait de masse molaire Ma : 29,0 g-molfl, Q 4. Déterminer l'expression de la pression P(z) de l'atmosphère en fonction notamment de l'altitude 2. Q 5. Évaluer la pression partielle en dioxygène à 11 km d'altitude (altitude de croisière typique pour un avion de ligne). On justifiera avec soin les valeurs numériques choisies intervenant dans cette évaluation. LB -- L'oxygène peut être conditionné en bouteille sous forme gazeuse a une pression de 200 bar ; on le trouve également stocké sous forme liquide. Dans les avions de transport de passagers, les masques à oxygène peuvent être reliés à des générateurs chimiques contenant du chlorate de sodium solide, de formule NaClOg. Celui--ci se décompose en chlorure de sodium NaCl et en dioxygène. Le déclenchement de la réaction se fait par percussion mécanique. Pour maintenir une vitesse de réaction suffisante, le chlorate de sodium doit être porté à 300 °C ; on ajoute donc du fer en poudre, dont l'oxydation produit la chaleur nécessaire. Les deux réactions s'écrivent 3 NaClO$--> NaCl(s) + äOg(g) (1.1) 3 2Fe(s) + äO2(g) _) FeZO3(S) (1.2) Les enthalpies libres standard (en kJ-mol"') de ces réactions dans le cadre de l'approximation d'Ellingham en fonction de la température (en K) sont respectivement A,Gî : --45,6 -- 0,275 T et A,.G3 : --824 + 0,220 T. Q 6. Pour un volume donné de contenant, évaluer le rapport masse de dioxygène gazeux à 200 bar ,. _ masse de dioxygène liquide à 20 °C des masses de dioxygène contenu dans un même volume, suivant qu'il est liquide (à 20 °C) ou gazeux (à 200 bar et 20 °C). Commenter le résultat. Q 7. Les réactions (1.1) et (1.2) sont--elles endo ou exothermiques ? Justifier. Q 8. Quelle relation y--a--t--il entre la variation d'enthalpie QP du système réactionnel dans les conditions isothermes et isobares, l'enthalpie standard de réaction A,.H ° et l'avancement de la réaction 5 '? Q 9. Rappeler l'expression de la constante d'équilibre d'une réaction en fonction de l'enthalpie libre stan-- dard de réaction et de la température. Q 10. Justifier que chacune des réactions (1.1) et (1.2) est totale dans les conditions d'utilisation des généra-- teurs chimiques (on admettra qu'ils produisent une pression partielle de dioxygène de l'ordre de 0,7 bar). Q 11. On suppose que la chaleur QP dégagée par la réaction (1.1) a 300 °C permet de chauffer adiabatique-- ment à une température Tf du chlorate de sodium, initialement seul a 20 °C, en quantité égale à celle consommée par la réaction (1.1). Déterminer Tf. Conclure quant à l'utilisation du fer. Q 12. Un générateur chimique prévu pour 4 passagers permet de délivrer 84 litres de dioxygène sous une pression de 0,70 bar à 20 °C. Évaluer la masse minimale de chlorate de sodium que contient ce générateur. 2018-03--10 09:37:17 Page 1/7 @@ BY--NC-SA II Pressurisation et conditionnement d'air dans la cabine d'un avion II.A * Pression dans la cabine. La cabine d'un avion est pressurisée : il s'agit, pendant le vol, de maintenir une pression supérieure a la pression rencontrée a 2500 m d'altitude dans l'« atmosphère standard ». Dans ce modèle, l'air est considéré comme un gaz parfait dont la composition chimique est indépendante de l'altitude et on considère que, dans la couche d'atmosphère située à moins de 11 km d'altitude, la température diminue de manière uniforme avec l'altitude au taux de 6,5 °C par kilomètre. Q 13. En considérant que la température vaut 20 °C à l'altitude 0 m, évaluer la pression partielle minimum en dioxygène dans la cabine d'un avion pendant le vol. Q 14. Il est couramment admis que l'air a la pression P0 = 1 bar est « respirable » si sa fraction molaire en dioxygène est supérieure a 16%. En déduire la pression partielle minimale en dioxygène qu'il faut assurer pour respirer confortablement et commenter le choix de pression de la question précédente. II.B * Conditionnement d'air dans la phase de croisière Le renouvellement de l'air de la cabine est essentiel au confort et a la sécurité des passagers. Pour maintenir un niveau suffisant d'oxygène, de l'air est prélevé a l'extérieur de l'avion. Cependant, cet air est trop froid pour être amené directement en cabine. Pour amener l'air extérieur à une température acceptable (en général réglable entre 18 et 26 °C), on utilise de l'air chaud en provenance des moteurs que l'on refroidit. Cet air froid est ensuite à nouveau mélangé à de l'air chaud avant d'être envoyé en cabine. On s'intéresse au système de climatisation pneumatique dont le principe de fonctionnement est présenté figure 1. De l'air provenant des moteurs et préalablement refroidi a 180 °C est amené en entrée de l'ACM (« Air Cycle Machine ») ; la pression de l'air entrant vaut P1 = 2,5 bar. Cet air est ensuite amené à T2 : 110 °C après avoir traversé un premier échangeur thermique, puis il est comprimé (T3 : 210°C), a nouveau refroidi dans un second échangeur thermique (T4 : 100 °C) et finalement détendu dans une turbine (T5 : 5 °C). air chaud air froid T, : 180 °C mm mm P1 : 2,5 bar E1 Compresseur Figure 1 Air Cycle Machine On fera les hypothèses de transformations adiabatiques réversibles pour l'air traversant le compresseur ou la turbine. L'air sera considéré comme un gaz parfait de coefficient "y : CI,/CU : 1,4. On rappelle que Cp et Cv sont des capacités thermiques massiques à volume et pression constants. Q 15. Citer des différences entre ce dispositif et un système de climatisation « classique ». Q 16. Déterminer la pression d'air en sortie du compresseur (P3), puis en sortie de la turbine (P5). Q 17. Rappeler, pour un écoulement stationnaire, l'expression du premier principe « industriel », ou premier principe de la thermodynamique en système ouvert, mettant en jeu des grandeurs massiques, en définissant avec précision les notations utilisées. Q 18. La puissance récupérée par la turbine est--elle suffisante pour entrainer le compresseur '? Q 19. Montrer qu'envoyer directement l'air issu du premier échangeur thermique dans la turbine ne permet pas de produire, à une pression suffisante, un air à la température de sortie de 5 °C. Q 20. Pourquoi ne se contente--t--on pas de refroidir l'air a l'aide d'un simple échangeur thermique '? III Analyseurs d'oxygène Il existe plusieurs techniques permettant de déterminer la proportion de dioxygène présent dans l'air ou dans un mélange gazeux. III.A * Analyseur d'oxygène à ooeyde de zirconium Certaines céramiques, comme celles constituées d'oxyde de zirconium ZrOQ, ont la propriété d'être conductrices d'électricité à haute température grâce au déplacement d'ions oxygène, de formule OZÎ Un disque d'oxyde de zirconium est monté entre le gaz à mesurer et un gaz de référence (l'air en général). Des électrodes sont reliées à chaque face du disque (figure 2). 2018--03--10 09:37:17 Page 2/7 («à BY--NC-SA Chambre de \\ Orifice d'entrée diffusion \\ du gaz a tester 02 i Cathode Oxyde de zirconium (V) 02 Anode Gaz de référence Figure 2 On admet que l'activité de l'ion 02* est la même a l'anode et à la cathode. Q 21. Écrire les demi--équations électroniques à l'anode et a la cathode. Q 22. Exprimer les deux potentiels d'électrodes en fonction des activités. En déduire la tension 6 entre la cathode et l'anode de la pile ainsi constituée. Q 23. Montrer que la fonction 6 : f (ln PO2) est une droite. Quel est l'intérêt d'avoir une réponse propor-- tionnelle a un logarithme ? Q 24. On considère que la cellule est chauffée à 650 0C. Que vaut 6 pour un mélange gazeux issu d'une combustion contenant 12 ppm (parties par millions : 1 ppm correspond a une fraction molaire égale à 10*6) de dioxygène ? On considère que les pressions sont égales à 1 bar de part et d'autre du disque de zirconium. Commenter le résultat. III.B * Sonde paramagnétique Cette sous--partie utilise les documents 1 et 2 fournis en annexe. III.B.1) Densité volumique de force magnétique Cette série de questions est en lien avec le document 1, en annexe. Q 25. Rappeler l'expression de la densité volumique d'énergie magnétique dans le vide en fonction notam-- ment de l'induction magnétique Ë Q 26. Qu'est--ce qu'un milieu magnétique « linéaire » '? Q 27. On rappelle que la force magnétique s'exerçant sur la partie mobile d'un milieu magnétique linéaire s'écrit Ë... \: grîle où Em est l'énergie potentielle d'interaction entre l'aimantation du milieu et le champ extérieur. A partir de l'expression (l) du document 1, donner l'expression de la densité volumique @... d'énergie d'aimantation du milieu paramagnétique dans le champ extérieur. Q 28. Justifier qu'une substance paramagnétique est attirée par les zones de champ magnétique élevé, alors qu'une substance diamagnétique est attirée par les zones de champ magnétique faible. III.B.2) Étude du fonctionnement de la sonde paramagnétique Cette série de questions est en lien avec le document 2, en annexe. La figure 3 représente le schéma de principe de la sonde paramagnétique étudiée. On précise que la position d'équilibre de l'haltère est choisie de façon a être légèrement décalée par rapport au plan de symétrie des aimants (qui correspond a un plan vertical). Le champ magnétique est supposé vertica' dans la zone où se situe l'haltère. < > pôle magnétique A boucle de rétroaction Module électronique ,? photodiodes photodiodes Principe de la boucle de rétroaction (vue de dessus) Figure 3 Sonde paramagnétique Q 29. Pourquoi les deux sphères sont--elles remplies de diazote '? Q 30. Montrer que, à l'équilibre, la pression du gaz sondé (contenant du dioxygène) est une fonction affine du carré du module du champ magnétique existant en ce point. On négligera le poids. 2018-03--10 09:37:17 Page 3/7 @@ BY--NC-SA Q 31. Évaluer la surpression dans l'air dont est responsable l'existence d'un champ magnétique B : 0,1 T. Q 32. La résultante des forces appliquées à chaque sphère de l'haltère est--elle orientée vers les régions de champ magnétique intense ou de champ magnétique faible '? Q 33. Expliquer alors pourquoi l'haltère tend à s'écarter de sa position d'équilibre lorsque du gaz contenant du dioxygène est introduit dans la cellule. Q 34. À l'aide d'un schéma sur lequel on fera figurer les forces en jeu et le sens du champ magnétique produit par les aimants, ainsi que le sens positif du courant dans la boucle de rétroaction, décrire le bilan de forces correspondant à l'équilibre de l'haltère lorsqu'il y a un courant passant dans la boucle de rétroaction. Q 35. Peut--on alors justifier la phrase « l'intensité du courant passant dans la spire est directement propor-- tionnelle a la concentration d'oxygène dans le mélange gazeux ». III.B.3) On s'intéresse dans cette série de questions au module électronique de la sonde. On propose le montage dont le schéma est donné figure 4, le module électronique étant constitué de l'association des trois unités entourées en pointillés. Chacune de ces 3 unités comporte un ALI supposé idéal et fonctionnant en régime linéaire. On note la présence de 4 résistances R, R1, R2 et R3, ainsi que d'un condensateur de capacité C. On donne par ailleurs en figure 5 la caractéristique intensité--tension d'une photodiode pour différentes puissances lumineuses reçues pour une longueur d'onde donnée (1140 nm). R1 C Il Il \\ >°° R2 _ a + A + |>OO i Ï % s. _ @ U + R3 ' Ë 1 % _ % ? 2 .'< % 15 3 @ unité 1 unité 2 unité 3 Figure 4 Module électronique 350 300 1 \> 250 +--èl-- 200 " 150 3 100 ÎË 50 CI) CJ fig 0 -- 0 mW ... -- 05 mW *50 * 10 mW _ 1 5 mW _1 1 00 _ 20 mW --150 -- 25 mW ; 30 mW --200 * 3,5 mW "250--2 --1,5 --1 --0,5 0 0,5 Tension (V) Figure 5 Caractéristique d'une photodiode 2018--03--10 09:37:17 Page 4/7 («à BY--NC-SA a) Les photodiodes Q 36. Comparer la caractéristique de la photodiode a celle d'une diode simple. Q 37. Une donnée essentielle d'une photodiode est sa sensibilité s (s > O) pour une longueur d'onde donnée qui est le rapport de l'intensité i du phot0c0urant (courant traversant la photodiode polarisée avec une tension u < 0) a la puissance lumineuse reçue. Que vaut la sensibilité de cette photodiode à 1140 nm '? On s'intéresse au montage des deux photodiodes sur le module électronique : on suppose qu'un pinceau lumineux incident de puissance 2,5 mW se divise en deux et que la photodiode Dl reçoit \}'Dl une puissance P1, le reste (P2) étant reçu par l'autre photodiode (figure 6). I est le phot0c0urant ] {>1 total produit par les deux photodiodes. > Q 38. Après avoir déterminé la tension aux bornes des deux photodiodes, tracer soigneuse-- l<\ ment la courbe représentant l'intensité ] en fonction de P1 -- P2 ; donner l'équation de cette D2\ courbe faisant intervenir le paramètre 5. Figure 6 Q 39. Quel est l'intérêt de ce montage a deux photodiodes '? b) Le module électronique Q 40. On note 0,2 la tension en sortie de l'unité 2. On assimile la tension en entrée de cette unité à un échelon de tension (à l'instant t = 0, la tension d'entrée prend une valeur constante E). Le condensateur est supposé initialement déchargé. Déterminer l'expression de u2(t). Comment nomme--t--on ce type de montage ? Q 41. Quel est le rôle de l'unité 3 ? Le montrer. Q 42. Exprimer l'intensité du courant de sortie is en fonction de la différence des puissances lumineuses reçues entre les deux photodiodes P1 -- PQ. R1 R2R30' Q 43. Le choix des dipôles permet d'ajuster la quantité Pourquoi cette quantité est--elle cruciale pour le bon fonctionnement de la mesure '? On peut ajouter sur l'unité 1 deux diodes montées comme indiqué sur la figure 7. La caractéristique de chacune de ces diodes est la même que celle des photodiodes D1 et D2, utilisées dans l'obscurité. % 31 m \\ _ >°° >: + {\ x\®Y Figure 7 Unité 1 modifiée Q 44. Représenter schématiquement la courbe u1 : f(1) de l'unité 1 ainsi modifiée. Quel est l'intérêt de cette modification '? III.B.4) Disposition des photodiodes Q 45. Faire deux schémas sur lequel on représentera le miroir, le pinceau lumineux qui l'éclaire, et les deux plaques photosensibles des deux photodiodes. On présentera deux situations : l'une correspondant a une position hors équilibre du miroir (on vient d'ajouter du dioxygène), l'autre a la position d'équilibre qui correspond a la prise de mesure. Q 46. Résumer en quelques phrases le fonctionnement du montage complet. 2018-03--10 09:37:17 Page 5/7 (CC) BY--NC-SA Annexe -- Document 1 Extrait de Compensation magnétique de pesanteur dans des fluides. synthèse des performances et contraintes par Alain MAILFERT, Daniel BEYSSENS, Denis CHATAIN et Clément LORIN Symposium de génie électrique, 8f9 juillet 2014, ENS Cachan Une distribution volumique de courant .Î (A-mä2) ou une répartition d'aimantation magnétique ]\7 (A-mÎ') dans un milieu matériel peuvent créer en tout point de l'espace un champ magnétique H (A-mÿ'). Des mesures de flux magnétique permettent de connaitre l'induction magnétique B (en T ou Wb m"), reliée à H dans le vide par B: uOH, où ;... est la splitéabilité du vide, et dans la matière par: B: uO(H + M). Les équations de Maxwell de la magnétostatique relient le champ H a ses deux sources possibles . div(B) : () d'où div(H) : --div(AÎ) _. r0t(H) : Î La création d'une aimantation ]\7 dans un milieu matériel provient, réciproquement, de l'application d'un champ magnétique ; il correspond a l'aimantation, une densité volumique d'énergie magnétique, d'où des densités de force magnétique quand le champ H varie avec la position. Dans les milieux dits linéaires, ]\7 : xH et B : u0(1 + x)H, où la constante x est la susceptibilité magnétique du milieu considéré. Les densités de forces volumiques ont alors l'expression simple : " H_0X f...= , g...d(Hz) <1> Les fluides intéressant les techniques spatiales sont soit paramagnétiques (oxygène liquide ou gazeux, avec X oe 10*3), soit diamagnétiques (hélium, hydrogène, eau, avec X 2 --10*6). L'obtention de forces importantes nécessite alors des valeurs élevées de grad(H2). « L'art >> du concepteur de sources de champ magnétique est alors interpellé... En outre, les susceptibilités étant en valeur absolue très petites devant 1, on écrit souvent avec une bonne approximation : " X 2 X ...----1"&dB--G 2 f ,,,Og ( >= % (> ! Remarque : les valeurs des susceptibilités magnétiques sont fournies à des températures très faibles. 7 Document 2 D'après Analyse d'oæyge'ne paramagnétique © Servomex 2014 Contrairement à la plupart des gaz, l'oxygène est fortement attiré par un champ magnétique puissant. Le principe d'une sonde paramagnétique s'appuie sur deux sphères de verres remplies d'azote qui sont assemblées sous la forme d'un haltère mobile suspendu à l'intérieur d'un champ magnétique. Un faisceau lumineux est projeté sur le miroir installé au centre de l'haltère. La lumière réfléchie est envoyée vers une paire de cellules photoélectriques. L'oxygène attiré vers le champ magnétique déplace les sphères d'azote et fait ainsi tourner l'haltère. Les cellules photoélectriques détectent le mouvement et produisent un signal qui passe par une boucle de contre--réaction. Cette boucle de contre--réaction fait passer un courant dans une spire placée autour de l'haltère. Cela provoque un effet de couple qui maintient l'haltère dans sa position initiale. L'intensité du courant passant dans la spire est directement proportionnelle à la concentration d'oxygène dans le mélange gazeux. 2018-03--10 09:37:17 Page (3/7 ,(cc BY--NC-SA Données Composition de la croûte terrestre Élément @ Si A1 Fe Ca Na K Mg Pourcentage (en masse) dans la croute terrestre 40,7 27,7 8,1 5,0 3,7 2,8 2,0 2,1 Masses molaires Élément ou composé H 0 N Fe Na0103 Masse molaire (gmolÿ') 1,01 16,0 14,0 55,8 106,4 Capacités thermiques massiques (supposées indépendantes de la température) Fe Na C103 Air (a press1on constante) Capacité thermique massique ... (J'kgÿl'Kÿl) 444 983 N 1000 Susceptibilités magnétiques de quelques gaz purs à température et pression ordinaires (300 K, 1 bar) Gaz 02 N2 H2 Ar _ --5,0 >< --1,7 >< --7,7 >< X 1,4 >< 10 7 10510 1040 10410 Loi de Nernst Pour l'exemple du couple oxydant / réducteur Ag+/Ag, le potentiel du couple s'écrit E : E° + %ln(a(Ag*)) où T représente la température en Kelvin et a(Ag+) est l'activité des ions Agf Données diverses Masse volumique du dioxygène liquide 1140 kg;mä3 Densité de l'eau de mer a 20 °C 1,03 Constante des gaz parfaits R : 8,31 J'Kfl-molf1 Constante de Faraday 1 F : 96 500 C-mÏ' Intensité du champ de pesanteur terrestre g : 9,81 N -kgfl lbar:1x105Pa oooFlNooo 2018-03--10 09:37:17 Page 7/7 @@ BY--NC-SA